 ��ҳ > ��Ѷ��̬ > ����ʴ� > һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ�����ⷽ��
��ҳ > ��Ѷ��̬ > ����ʴ� > һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ�����ⷽ��һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ�����ⷽ��
B1 ��Ʒ�ɼ�����Ʒ����
������ͬһ���ŵ����������װ�����ٳ�ȡ12����С���۰�װ��Ʒ��1��4��Ʒ���ڼ�⣬1��4��Ʒ������������1��2��Ʒ���ɾ͵ط�棩��Ҫʱ���ڸ��졣��������С���۰�װ��Ӧ�����ѣ�����ǰ����������
��100�������������������������ڼ�������3����װ����ÿ����װ��ȡ����ȷ��ȡ10 g±1g��Ʒ���������뵽200 mL���������ˮ�У���ֻ��ȣ��õ�һ��������ˮ��Һ��Һ���Ʒ��ԭҺֱ������Һ��
�类����Ʒ���д�����ˮ��֬���϶����²��������㹻��Һʱ��ϡ��Һ���ɰ�ÿ��50mL������ֱ���������㹻��������Һ���ڼ���ϸ�����������������������ʱӦ����ϡ�Ͷȡ�
B2 ϸ�������������ʼ��Ⱦ����ⷽ��
�����������ڲ�Ʒ��ʼ��Ⱦ����ϸ����������������ͳ��Ϊϸ��������������⡣
B2.1 ��������
������������ˮ��Һ��Ȼ������ȡ����Һ�����������������5��ƽ��ÿ��ƽ���м���1 mL��Һ��Ȼ������ȴ��45�����ҵ��ۻ���Ӫ����֬������15 ��20mL����ÿ��ƽ���ڻ�Ͼ��ȡ�����֬���̺�תƽ����35��±2�� ����48h����ƽ���ϵľ�������
B2.2 �������
�����Ƭ״������ƽ�岻�˲��ã���������Ҫ���ƽ���ϵľ��䣬��ʽ(B1)��������
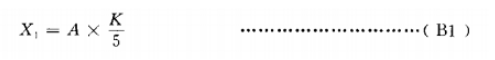
ʽ�У�X1�D�Dϸ������������cfu/g��cfu/mL��
A�D�D5��Ӫ����֬������ƽ���ϵ�ϸ������������
K�D�Dϡ�Ͷȡ�
����������100���ڣ���ʵ�������棬����100ʱ���ö�λ��Ч���֡�
�����Ʒ�����������������Ĺ涨����B2.3���и���ͽ�����档
B2.3 ���췽��
������ĸ�����Ʒ��ǰ������2�Σ�2�ν��ƽ��ֵ���ﵽ�����Ĺ涨�����ж�������Ʒ�ϸ��������κ�1�ν��ƽ��ֵ���������涨�����ж�������Ʒ���ϸ�
B3 ��Ⱥ��ⷽ��
B3.1 ��������
ȡ��Һ5mL����50mL���ǵ��η��ܣ���35��±2�� ����24 h���粻����Ҳ����������Ϊ��Ⱥ���ԡ�
�����������������߽�������������֬ƽ�壬��35��±2������18��24 h���۲�ƽ���Ͼ�����̬�����͵Ĵ���Ϊ����ɫ�����ɫ��Բ�Σ���Ե���룬����⻬ʪ�����н�������Ҳ�еij��Ϻ�ɫ���������Դ���������ۺ�ɫ�����Ľ���ľ��䡣
����ȡ���ƴ���1��2����������Ⱦɫ���죬ͬʱ�������Ƿ��ܣ���35��±2������24 h���۲���������
B3.2 �������
�����ǵ��η��ܲ�����������Ƿ��ܲ������������������ƽ�����е��ʹ��䣬������ȾɫΪ������ѿ���˾����ɱ��汻����Ʒ����˾���
B4 ��ŧ�˾���ⷽ��
B4.1 ��������
ȡ��Һ5 mL�����뵽50 mL SCDLP����Һ�У���ֻ��ȣ���35��±2������18��24 h��������ŧ�˾�����������Һ�������һ�㱡��Ĥ������Һ���ʻ���ɫ������ɫ��������Һ�ı���Ĥ����ȡ��������߽���ʮ���������廯���֬ƽ�壬��35��±2������18��24 h���۲������������ŧ�˾��ڴ����������������ã������ƽ����Ե������������Χ�������Դ��ۺ�ɫ��������������
����ȡ���ɾ���ͿƬ��������Ⱦɫ������Ϊ���������Ծ���Ӧ�����������飺
��������ø���飺ȡһС��ྻ�İ�ɫ��ֽƬ�������ƽ���ڣ�����������ȡ���ɾ���Ϳ����ֽƬ�ϣ�Ȼ�������ϵμ�һ�������Ƶ�1�������Ա�������Һ��30 s�ڳ��ַۺ�ɫ���Ϻ�ɫ��Ϊ����ø�������ԣ�����ɫ��Ϊ���ԡ�
������ŧ�������飺ȡ2��3�����ɾ��䣬�ֱ��������ŧ���زⶨ��������б�棬35��±2������24 h���������ȼ���3��5 mL�������ʹ�������п��ܴ��ڵ���ŧ�����ܽ⣬�����ȼ������ɫʱ���������Ƶ���һ�Թ��в�����1 mol/L������1 mL������Ƭ�̡����ϲ���ַۺ�ɫ���Ϻ�ɫ��Ϊ���ԣ���ʾ����ŧ���ش��ڡ�
���������λ�ԭ�������飺��ȡ��������������������������ˮ�������У���35��±2������24 h��������С������������Ϊ���ԡ�
��������Һ�����飺ȡ���ɾ��䴿��������̽����������������ڣ���35��±2������24h��ȡ������4��10�棬���Գ�Һ̬Ϊ���ԣ�������Ϊ���ԡ�
����42���������飺��ȡ�����������������ͨ��֬б���������ϣ���42������24��48 h������ŧ�˾�����Ϊ���ԡ�
B4.2 �������
������Ʒ����������������֤ʵΪ���������Ը˾�������ø����ŧ�˾������Ϊ�����ߣ����ɱ��汻����Ʒ�м����ŧ�˾�������ŧ�����������Զ�Һ�������������λ�ԭ������42�������������߽�Ϊ����ʱ���Կɱ��汻����Ʒ�м����ŧ�˾���
B5 ���ɫ���������ⷽ��
B5.1 ��������
ȡ��Һ5 mL�����뵽50 mL SCDLP����Һ�У���ֻ��ȣ���35��±2������24 h��
��������������Һ��ȡ1��2���ֻ������߽�����Ѫ��֬�������ϣ���35��±2������24��48 h����Ѫ��֬ƽ���ϸþ�����ʽ��ɫ�����ͻ��Բ�Σ�����������⻬����Χ����ѪȦ��
������ȡ���;��䣬ͿƬ��������Ⱦɫ���죬���ɫ�������Ϊ������������������г�����״����ѿ�����Ĥ������������������Ӧ�����������飺
������¶���������飺ȡ����������ָ�¶������Һ����35��±2������24 h������¶��������Ϊ���ԡ�
����Ѫ������ø���飺��Ƭ����ȡ�������ز�Ƭ��һ�˵μ�һ��������ˮ����һ�˵μ�һ����Ѫ������ȡ����ֱ���������ˮ��Ѫ����ϣ�5 min��Ѫ���ڳ����ſ�����״���飬����ˮ���Գʾ��Ȼ�����������Ϊ���ԣ������߾���������Ϊ���ԡ�����ˮ����Ѫ���ξ������������ٽ����Թ�����ø���飻�Թܷ�����ȡ1��4����Ѫ��0.5 mL�������С�Թ��У�������������24 h����������0.5 mL�����ȣ���35��±2�������ˮԡ�У�ÿ��Сʱ�۲�һ�Σ�24 h֮�ڳ������鼴Ϊ���ԡ�ͬʱ����֪Ѫ������ø���Ժ����Ծ��������������0.5 mL�����������Զ��ա�
B5.2 �������
������֬ƽ�����п��ɾ�������������Ϊ����������������������ܷ���¶�����ᣬѪ������ø���������ߣ��ɱ��汻����Ʒ������ɫ���������
B6 ��Ѫ���������ⷽ��
B6.1 ��������
ȡ��Һ5 mL���뵽50 mL������������35��±2������24 h��
�����������ﻮ�߽���Ѫ��֬ƽ�壬35��±2������24 h�۲������������Ѫ���������Ѫƽ����Ϊ�Ұ�ɫ���������������״ͻ�𣬱���⻬����Ե���룬��Χ����ɫ����ѪȦ��
������ȡ���;�����ͿƬ������Ⱦɫ���죬ӦΪ���������ԣ�����״���е����������������������Ӧ�����������飺
����ø���飺��ȡ�����Ѫ��0.2 mL(0.01 g����ؼ�5 mL��Ѫ�����ȣ������ij�������ȡ����Һ)������0.8 mL���������ˮ�����Ⱥ��ټ�������24 h����������0.5 mL��0.25���Ȼ���0.25 mL�����ȣ���35��±2��ˮԡ�У�2 min�۲�һ��(һ��10 min�ڿ�����)����Ѫ�����̺�����۲첢��¼�ܻ�ʱ�䡣��2 h�ڲ��ܻ�����������24 h�۲죬������ȫ���ܻ�Ϊ���ԣ�24 h�Բ��ܻ�Ϊ���ԡ�
�����˾����������飺���������ҺͿ��Ѫƽ���ϣ����������ȡÿƬ��0.04��λ�˾��ĵ�ֽƬ����ƽ������ϣ�ͬʱ����֪���Ծ��������գ���35��±2���·���18��24 h�����־�����Ϊ���ԡ�
B6.2 �������
���������������״���������Ѫƽ���ϳ�����ѪȦ������ø�˾����������ԣ��ɱ��汻����Ʒ�����Ѫ���������
B7 �������������ⷽ��
B7.1 ��������
������������ˮ��Һ��Ȼ������ȡ����Һ�����������������5��ƽ��ÿһ��ƽ���м���1mL��Һ��Ȼ������ȴ��45�����ҵ��ۻ���ɳ����֬������15��25 mL����ÿ��ƽ���ڻ�Ͼ��ȣ���֬���̺�תƽ����25��±2������7�죬�ֱ���3��5��7��۲죬����ƽ���Ͼ�������������־������ӣ���ǰһ�εľ������Ϊ��
B7.2 �������
�����Ƭ״������ƽ�岻�˲��ã���������Ҫ���ƽ���ϵľ��䣬��ʽ��B2����������
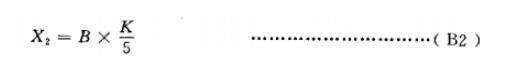
ʽ�У�X2�D�D�������������cfu/g��cfu/mL��
B�D�D5��ɳ����֬������ƽ���ϵ��������������
K�D�Dϡ�Ͷȡ�
����������100���ڣ���ʵ�������棬����100ʱ���ö�λ��Ч���֡�
�����Ʒ�����������������Ĺ涨����B7.3���и���ͽ�����档
B7.3 ���췽��
������ĸ�����Ʒ��ǰ������2�Σ�2�ν�����ﵽ�����Ĺ涨�����ж�������Ʒ�ϸ��������κ�1�ν�����������涨�����ж�������Ʒ���ϸ�
B8 ������Լ�ⷽ��
B8.1 ��������
ȡ��Һ5mL���뵽50mLɳ���������У�25��±2������7�죬���չ۲��������������
B8.2 �������
�����ܻ���Ӧת��ɳ����֬��������֤ʵ������������ɱ��汻����Ʒ��������
����ͼƬ��Դ�����磬������Ȩ������ϵ�ͷ�ɾ��
 GB 15979-2002һ����ʹ��������Ʒ��������ȫ�ģ�
GB 15979-2002һ����ʹ��������Ʒ��������ȫ�ģ� һ����ʹ��������Ʒ�Ķ��壿
һ����ʹ��������Ʒ�Ķ��壿 һ����ʹ��������Ʒ��������ָ��
һ����ʹ��������Ʒ��������ָ�� һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ����ѧ���Է���
һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ����ѧ���Է��� һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ�����ⷽ��
һ����ʹ��������Ʒ�����֡�ʪ����ֽ�������ף���Ʒ�����ⷽ�� ���ϻ�����ҽ����ƿ��ּ������ Ϊ��������ṩ��������
���ϻ�����ҽ����ƿ��ּ������ Ϊ��������ṩ�������� ����������ɫͨ��������ּ��̰� 5�ҿ��ַ�����Ʒ��ҵ��������
����������ɫͨ��������ּ��̰� 5�ҿ��ַ�����Ʒ��ҵ�������� ����ʡ�����߱����ֺͷ���������ؼ�������ļ������������
����ʡ�����߱����ֺͷ���������ؼ�������ļ������������ ���������족���ֿ��������������
���������족���ֿ�������������� ɽ��ʡҽ����е������ľ߱�ҽ�ÿ��ֺ�ҽ�÷������������
ɽ��ʡҽ����е������ľ߱�ҽ�ÿ��ֺ�ҽ�÷������������

 ȫ���������ߣ�
ȫ���������ߣ�